铬酸,化学式为HCrO,是三氧化铬溶于硫酸以及铬酸盐/重铬酸盐酸化时生成的化合物之一。其仅仅存在于溶液中,由三氧化铬溶于水中而得。铬酸洗液是实验室常用的清洗液,兼有酸性和氧化性,可以去除实验仪器内壁和外壁的污垢及难溶物质。
精选百科
本文由作者推荐
铬酸相关的文章
蚜虫(英文名:Aphid),是球蚜总科(Adelgoidea)和蚜总科(Aphidoidea)昆虫的统称,又称腻虫、密虫,隶属于节肢动物门昆虫纲半翅目,包括球蚜科、根瘤蚜科、纩蚜科、平翅绵蚜科、扁蚜科、瘿绵蚜科、群蚜科、毛管蚜科、斑蚜科、毛蚜科、大蚜科、短痣蚜科和蚜科。蚜虫体长0.5~7.5mm,大
刘慈欣谈科幻《刘慈欣谈科幻(第1辑)》有作者在创作科幻小说时的心路历程,有作者对一些经典科幻作品的精彩书评、影评,还有一些对话与访谈,折射出作者作为一个科幻迷对科幻、对未来的看法,也展现出科幻作家独特的浪漫主义情怀。
帖木儿本词条是多义词,共2个义项帖木儿帝国创建者帖木儿(波斯-阿拉伯文:تیمور,拉丁转写:Tēmōr,1336.4.9—1405.2.18),帖木儿帝国创建者(1370.4.10—1405.2.18在位)。绰号“帖木儿兰”(跛足帖木儿)出身突厥化的蒙古贵族。早年臣属于河中统治者合札罕及东察合台汗秃忽鲁帖木儿。1362年,与内兄忽辛起兵反抗察合台贵族,通过扶持傀儡的方式分治河中。1370年,杀死
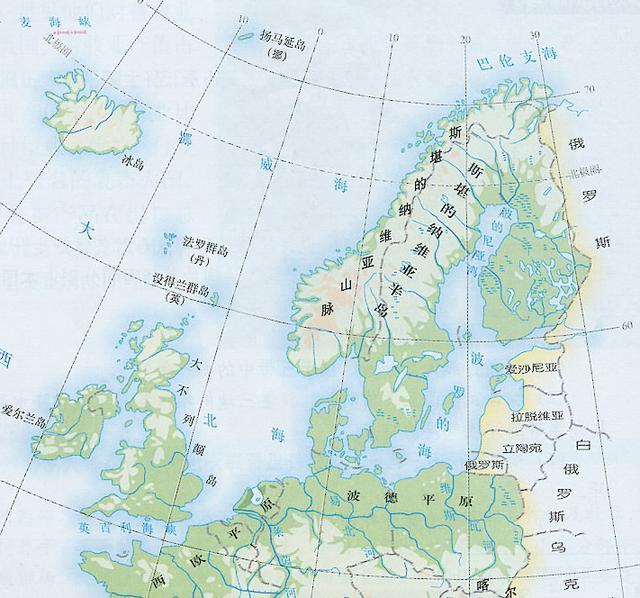
斯堪的纳维亚半岛(丹麦语:Skandinaviske halvø,瑞典语:Skandinaviska halvön,挪威语:Den skandinaviske halvøy,芬兰语:Skandinavian niemimaa),位于欧洲西北角,其濒临波罗的海、挪威海及北欧巴伦支海,与俄罗斯和芬兰北部接壤,北至芬兰,意为“斯堪的纳维亚人居住之地”。“斯堪的纳维亚”(Scandinavian)一词源自条顿语“skadino”,意为“黑暗”,再加上表示领土的后缀-via,全名意为“黑暗的地方”。因半岛 地处高纬

尚可名片
这家伙太懒了,什么都没写!
作者