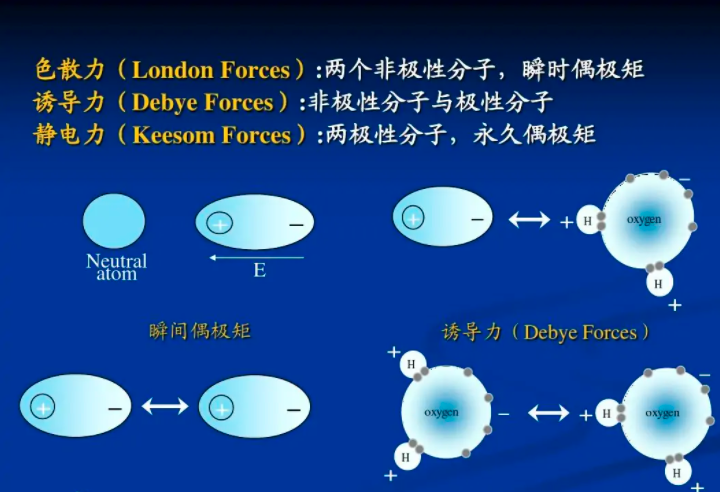
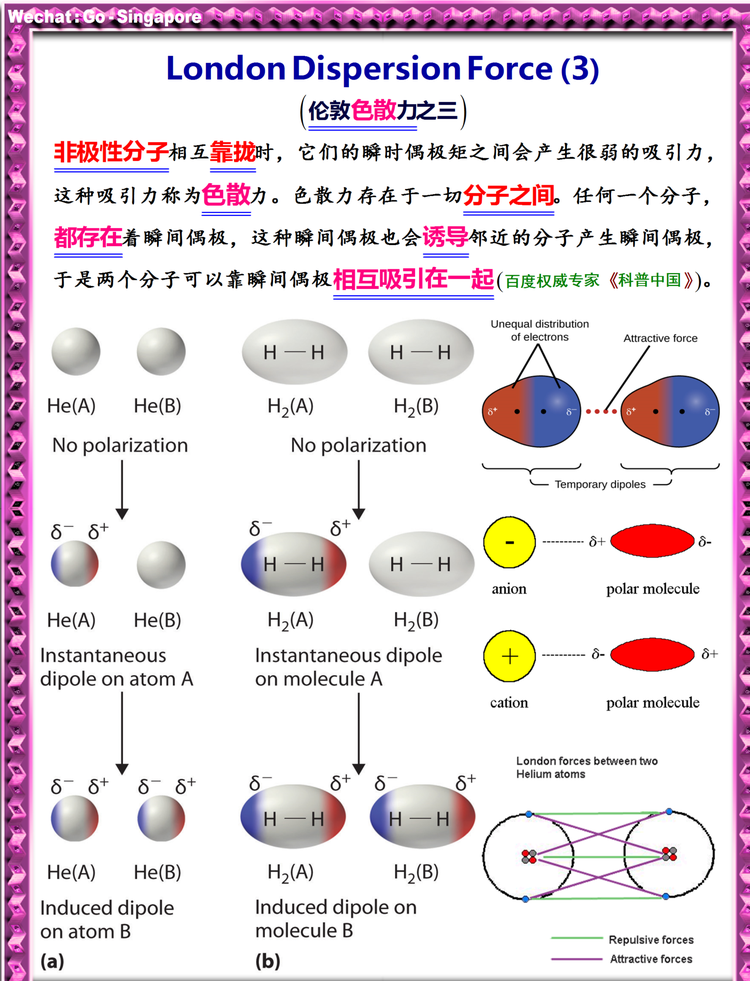
非极性分子相互靠拢时,它们的瞬时偶极矩之间会产生很弱的吸引力,这种吸引力称为色散力。色散力存在于一切分子之间。任何一个分子,都存在着瞬间偶极,这种瞬间偶极也会诱导邻近分子产生瞬间偶极,于是两个分子可以靠瞬间偶极相互吸引在一起。这种瞬间偶极产生的作用力称为色散力(dispersion force)。色散力是伦敦(London)于1930年根据近代量子力学方法证明的,由于从量子力学导出的理论公式与光色散公式相似,因此把这种作用称为色散力,又叫做伦敦力。
色散力相关的文章
脑膜炎是脑膜的弥漫性炎症性改变。由细菌、病毒、真菌、螺旋体、原虫、立克次氏体、肿瘤与免疫相关的各种炎性因子侵犯脑膜引起。具体发病机制不明确。脑膜炎可累及硬脑膜、蛛网膜和软脑膜。脑脊髓膜炎有3种基本类型:化脓性脑膜炎、淋巴细胞性脑膜炎(多由病毒引起)、非化脓脑膜炎(可由结核杆菌、梅毒螺旋体、布鲁氏菌及
脑血管病是指脑部血管的各种疾病引起脑组织的缺血或出血性损伤,包括脑动脉粥样硬化、血栓形成、脑血管狭窄或闭塞、脑动脉炎、脑动脉损伤、脑动脉瘤、颅内血管畸形、脑动静脉瘘等。脑血管病的病因包括血脂异常、动脉粥样硬化、脂肪透明样变性纤维蛋白坏死、纤维肌肉发育不良、血管淀粉样变、血管炎、静脉血栓、血管痉挛等。
华南地区(英文名:South China),简称华南,位于中国南部,北与华中区、华东区相接,南濒南海,西南与越南相邻。面积约45万平方千米,约占中国陆地总面积的4.7%。该区经纬度范围为18°一30°N,96°一118°E。全区海岸线长约1万千米,岛屿数目不低于2200座。该区在行政区划上普遍包括台
洪凌波,是金庸小说《神雕侠侣》中的角色,是赤练仙子李莫愁的嫡传弟子,陆无双的师姊。洪凌波相貌挺美,武功不弱,她长期伴随在师父左右,有时代师出手杀人,陪同师父一起闯荡江湖,客观上为发挥古墓派威名起到一定作用。她在一出场奉李莫愁之命来杀陆氏一门时提到她不过十五六岁年龄,所以应该和小龙女相仿或略小一些,比
阿姆斯特丹(Amsterdam),荷兰首都及最大城市,人口约110万,位于荷兰西部的北荷兰省。享誉世界的旅游城市和国际大都市,在最新的世界城市排名权威机构GaWC中名列欧洲第三,仅次于伦敦和巴黎。
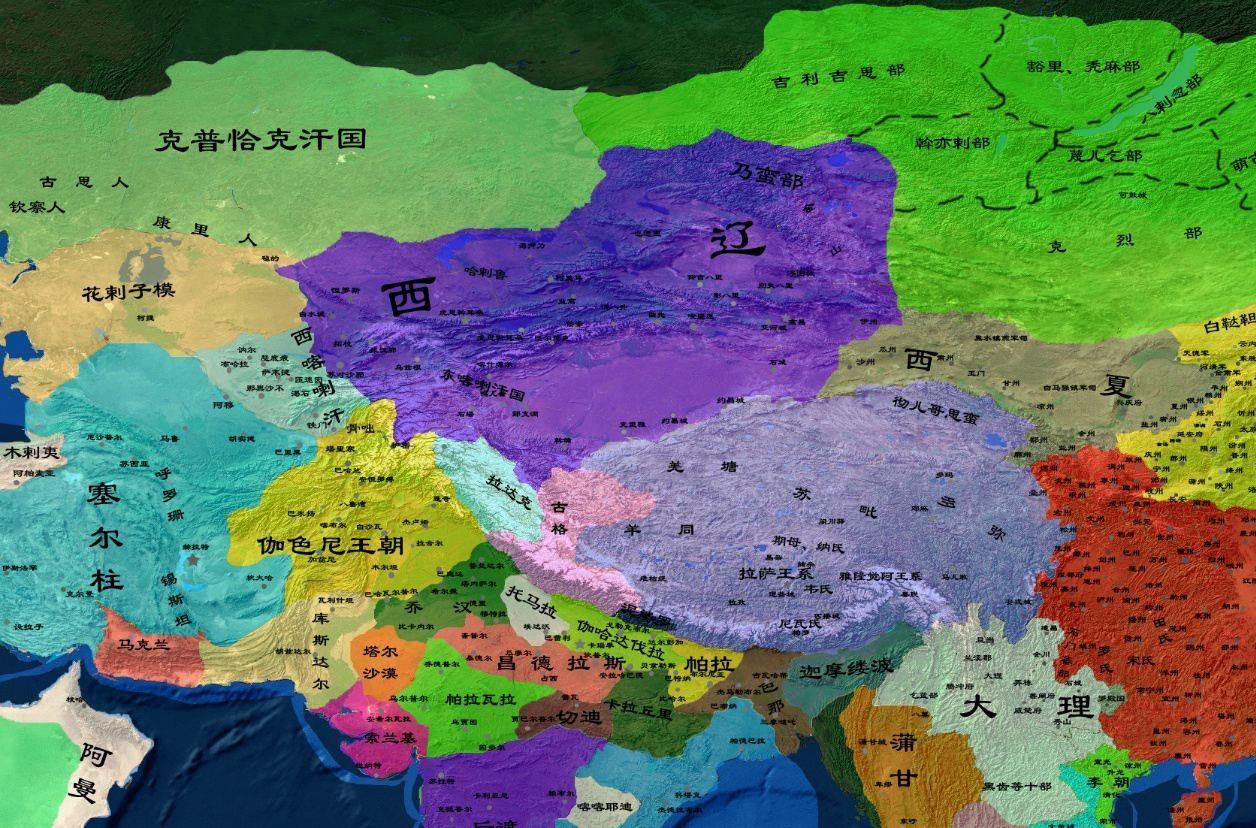
西辽(1124年~1218年)是中国历史上由契丹族在中国新疆和中亚地区建立的政权,历三世三帝二后,享国八十八年。西辽的建立者耶律大石是辽朝开国皇帝耶律阿保机的八世孙。耶律大石原本效力于天祚帝,在辽朝即将灭亡之际出奔。1124年,耶律大石称王,到达可敦城(今蒙古国布尔干省青托罗盖古回鹘城)建立根据地。1132年,耶律大石在叶密立城登基称帝,号“菊儿汗”,群臣又尊汉号为“天祐皇帝”,建元延庆,西辽正式建立。随后耶律大石向西域、漠北、中亚等地区扩张,建都于虎思斡鲁朵(今吉尔吉斯斯坦托克玛克东南布拉纳)。在114

尚可名片
这家伙太懒了,什么都没写!