精选百科
本文由作者推荐
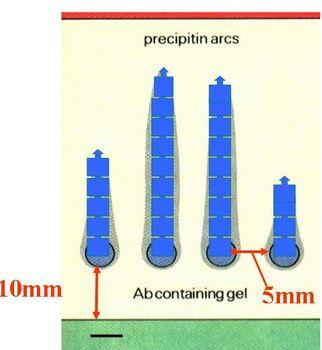
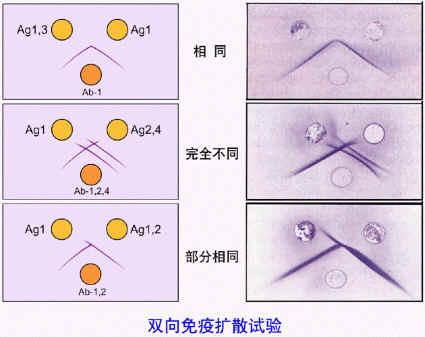
酶免疫电泳相关的文章
电影《被嫌弃的松子的一生》(日语:嫌われ松子の一生)改编自山田宗树所著同名小说,由中岛哲也编剧、导演,石田雄治、佐谷秀美、间濑泰宏、小玉圭太等主演,于2006年5月27日在日本首映。
奥马尔·哈桑·艾哈迈德·巴希尔(阿拉伯语:عمرحسناحمدالبشي,1944年1月1日-),男,出生于苏丹北部尼罗河省,苏丹军事领导人、政治家,苏丹第7任总统,毕业于喀土穆苏丹军事学院。
阿拉伯国家联盟(League of Arab States)是为了加强阿拉伯国家联合与合作而建立的地区性国际组织。是当今世界上最早成立的地区性组织。简称阿拉伯联盟或阿盟。
阿姆斯特丹(Amsterdam),荷兰首都及最大城市,人口约110万,位于荷兰西部的北荷兰省。享誉世界的旅游城市和国际大都市,在最新的世界城市排名权威机构GaWC中名列欧洲第三,仅次于伦敦和巴黎。
立原透耶作家立原透耶,有作品约30部。其作品以“轻小说”为主,著有《冥界武侠谈》系列和《CITY VICE》系列等,同时涉足奇幻、科幻、恐怖等领域。另著有《苦思乐西游传》、《迷镜楼》等短篇。其作品《卖梦的小孩子》获得1991年集英社cobalt读者大奖。其短篇小说曾经被翻译成意大利语和英语等。

尚可名片
这家伙太懒了,什么都没写!
作者