结构
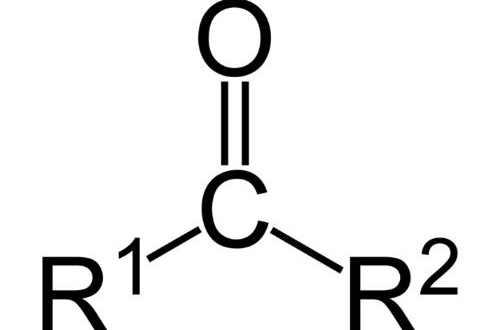
结构式
结构简式:(—CO—)
使含该结构的有机物有还原性
如:草酸

在生物中,另有专业名称,羰基。
分子轨道有机化学中,羰基化合物指的是一类含有羰基的化合物。
由一个

或sp杂化(见杂化轨道)的碳原子与一个氧原子通过双键(见化学键)相结合而成的基团,可以表示为:关系式
羰基

的双键的键长约1.22埃(公制长度单位,一亿分之一厘米,常用以表示光波的波长及其他微小长度)。由于氧的电负性(3.5)大于碳的电负性(2.5),C=O键的电子云分布偏向于氧原子:这个特点决定了羰基的极性和化学反应性。
构成羰基的碳原子的另外两个键,可以单键或双键的形式与其他原子或基团相结合而成为种类繁多的羰基化合物。羰基化合物可分为醛酮类和羧酸类两类(R为烷基):
构成羰基的碳原子的另外两个键,可以单键或双键的形式与其他原子或基团相结合而成为种类繁多的羰基化合物。羰基化合物可分为醛酮类和羧酸类两类(R为烷基):
醛酮类:

醛
酮羧酸类:

羧酸
羧酸酯
酸酐
酰基过氧化物
酰胺
酰卤
烯酮
异氰酸酯由于碳原子和氧原子的电负性差别,羰基化合物容易与亲核试剂发生亲核加成反应。
羰基的性质很活泼,容易起加成反应,如与氢生成醇。
簇合物中的键结模式
在羰基簇合物化学中,羰基配体有许多不同的键结模式。大部分常见的羰基配体都是端接配体,但羰基也常连接2个或3个金属原子,形成μ或μ的桥接配体。有时羰基中的碳和氧原子都会参与键结,例如μ-η就是一个哈普托数为2,连接3个金属原子的桥接配体。
金属中心原子形成反馈π键使M-C键能增强,同时活化了-C-O键。
性质
物理性质:具有强红外吸收。
化学性质:由于氧的强吸电子性,碳原子上易发生亲核加成反应。其它常见化学反应包括:亲核还原反应,羟醛缩合反应。
特征
在进行金属羰基配合物的分析时,常会使用红外吸收光谱法。在一氧化碳气体,C-O键的振动(一般以νCO表示)出现在光谱中2143cm的位置。νCO的位置和金属和碳之间键结强度呈现负相关的关系。
| CO | 2143 |
| Ti(CO)6 | 1748 |
| V(CO)6 | 1859 |
| Cr(CO)6 | 2000 |
| Mn(CO)6 | 2100 |
展开表格除了振动的频率外,频谱中νCO的个数也可用来分析配合物的结构,八面体结构旳配合物(如Cr(CO)6),其频谱只有一个νCO。对称性较弱的配合物,其频谱也会比较复杂。
如Fe2(CO)9的光谱中,CO键的振动频率就出现在2082,2019,1829cm。
在簇合物中也可以用νCO看出CO配基的配位方式。
桥接(μ)的羰基配体其νCO会比一般端接的羰基配体低100-200cm。μ的羰基配体其νCO会更低。以下是典型铑簇合物的νCO:
| Rh2(CO)8 | 2060,2084 | 1846,1862 | |
| Rh4(CO)12 | 2044,2070,2074 | 1886 | |
| Rh6(CO)16 | 2045,2075 | | 1819 |
羟醛缩合(1)羟醛缩合
在稀碱或稀酸的作用下,两分子的醛或酮可以互相作用,其中一个醛(或酮)分子中的α-氢加到另一个醛(或酮)分子的羰基氧原子上,其余部分加到羰基碳原子上,生成一分子β-羟基醛或一分子β-羟基酮。这个反应叫做羟醛缩合或醇醛缩合(aldolcondensation)。通过醇醛缩合,可以在分子中形成新的碳碳键,并增长碳链。
羟醛缩合反应历程,以乙醛为例说明如下:
第一步,碱与乙醚中的α-氢结合,形成一个烯醇负离子或负碳离子:
第二步是这个负离子作为亲核试剂,立即进攻另一个乙醛分子中的羰基碳原子,发生加成反应后生成一个中间负离子(烷氧负离子)。
第三步,烷氧负离子与水作用得到羟醛和OH。
稀酸也能使醛生成羟醛,但反应历程不同。酸催化时,首先因质子的作用增强了碳氧双键的极化,使它变成烯醇式,随后发生加成反应得到羟醛。
生成物分子中的α-氢原子同时被羰基和β-碳上羟基所活化,因此只需稍微受热或酸的作用即发生分子内脱水而生成,α,β-不饱和醛。
凡是α-碳上有氢原子的β-羟基醛、酮都容易失去一分子水。这是因为α-氢比较活泼,并且失水后的生成物具有共轭双键,因此比较稳定。
除乙醛外,由其他醛所得到的羟醛缩合产物,都是在α-碳原子上带有支链的羟醛或烯醛。羟醛缩合反应在有机合成上有重要的用途,它可以用来增长碳链,并能产生支链。
具有α-氢的酮在稀碱作用下,虽然也能起这类缩合反应,但由于电子效应、空间效应的影响,反应难以进行,如用普通方法操作,基本上得不到产物。一般需要在比较特殊的条件下进行反应。例如:丙酮在碱的存在下,可以先生成二丙酮醇,但在平衡体系中,产率很低。如果能使产物在生成后,立即脱离碱催化剂,也就是使产物脱离平衡体系,最后就可使更多的丙酮转化为二丙酮醇,产率可达70%~80%。二丙酮醇在碘的催化作用下,受热失水后可生成α,β-不饱和酮。
在不同的醛、酮分子间进行的缩合反应称为交叉羟醛缩合。如果所用的醛、酮都具有α-氢原子,则反应后可生成四种产物,实际得到的总是复杂的混合物,没有实用价值。一些不带α-氢原子的醛、酮不发生羟醛缩合反应(如

、

、
、
r、
等),可它们能够同带有α-氢原子的醛、酮发生交叉羟醛缩合,其中主要是苯甲醛和甲醛的反应。并且产物种类减少,可以主要得到一种缩合产物,产率也较高。反应完成之后的产物中,必然是原来带有α-氢原子的醛基被保留。在反应时始终保持不含α-氢原子的甲醛过量,便能得单一产物。芳香醛与含有α-氢原子的醛、酮在碱催化下所发生的羟醛缩合反应,脱水得到产率很高的α,β-不饱和醛、酮,这一类型的反应,叫做克莱森-斯密特(Claisen-Schmidt)缩合反应。在碱催化下,苯甲醛也可以和含有α-氢原子的脂肪酮或芳香酮发生缩合。另外,还有些含活泼亚甲基的化合物,例如丙二酸、丙二酸二甲酯、α-硝基乙酸乙酯等,都能与醛、酮发生类似于羟醛缩合的反应。卤代反应(2)烃基上的卤代反应
由于羰基强烈的吸电子作用,醛、酮的α-氢原子容易被卤素取代,生成α-卤代醛、酮。
这类反应可以被酸或碱催化。用酸催化时,可通过控制反应条件(例如酸和卤素的用量,反应温度等),使所得的产物主要是一卤代物,二卤代物或三卤代物。
决定整个反应速度的步骤是生成烯醇的步骤,即取决于丙酮和酸的浓度,而与卤素的浓度无关。
生成的一卤代物继续与卤素反应的速度降低。这是由于卤素原子电负性很大,使一卤代物烯醇式双键上的电子云密度降低,因而与卤素的亲电加成难以进行。所以酸催化卤代反应常停止在一卤代产物上。
碱催化的卤代反应中决定整个反应速度的步骤是生成负碳离子(烯醇负离子)的步骤,即反应速度与丙酮和碱的浓度有关,与卤素的浓度无关。
用碱催化时,则因反应速度很快,一般不能使反应控制在生成一卤代物或二卤代物阶段。这是因为当一个卤素原子引入α-碳原子以后,由于卤素是吸电子的,使得α-氢原子更加活泼,形成新的负碳离子更加容易,形成的负碳离子更加稳定,因此⑴式反应更快,这就是碱催化难以控制在一卤代物的原因。
凡结构式为

的醛或酮(乙醛和甲基酮)与次卤酸或卤素碱溶液作用时,甲基上的三个α-氢原子都被卤素原子取代,生成三卤代衍生物。而这种三卤代衍生物,由于卤素的强吸电子诱导效应,使碳的正电性大大加强,在碱的存在下,发生碳碳键的断裂,分解生成三卤甲烷(俗称卤仿)和羧酸盐。因此,通常把次卤酸钠的碱溶液与乙醛或甲酮作用,α-甲基的三个氢原子都被卤素原子取代,生成的三卤衍生物在受热时,其碳碳键断裂,生成卤仿和羧酸盐的反应称为卤仿反(haloformareaction)。由于次卤酸钠是一个氧化剂,它可以使具有
结构的醇氧化变成为含-COCH3结构的醛或酮。因此,凡含有
结构的醇也都能发生卤仿反应。如果用次碘酸钠(碘加氢氧化钠)作试剂,生成难溶于水的且具有特殊臭味黄色结晶碘仿(CHI)的反应称为碘仿反应。
因而常用这个反应来鉴别具有

结构的醛、酮和具有
结构的醇。《中华人民共和国药典》即利用此反应来鉴别甲醇和乙醇。甲基酮的卤仿反应是制备羧酸的一个途径。另外,由于次卤酸盐对于双键没有干扰,所以一些不饱和的甲基酮也可以通过卤仿反应转变为相应的羧酸。
反应
羰基(酮基)的亲核加成反应
基本介绍羰基中的π键和碳碳双键中的π键相似,也易断裂,因此与碳碳双键类似,羰基也可以通过断裂π键而发生加成反应。与碳碳双键不同的是,由于羰基氧原子的电负性比碳原子大,易流动的π电子被强烈地拉向氧原子,所以羰基的氧原子是富电子的,以致氧原子带部分负电荷,羰基的碳原子是缺电子的,使碳原子带部分正电荷(),所以羰基是一个极性基团,具有一定的偶极矩,偶极矩的方向由碳指向氧,使得羰基具有两个反应中心,在碳原子上呈现正电荷中心,在氧原子上呈现负电荷中心。一般地讲,带部分正电荷的碳原子比带负电荷的氧原子具有更大的化学反应活性。因此,与碳碳双键易于发生亲电加成反应不同,碳氧双键最易发生被亲核试剂进攻的亲核加成反应。一般是亲核试剂(NuA)的亲核部分(Nu)首先向羰基碳原子进攻,其次带正电荷的亲电部分(A)加到羰基的氧原子上。所以,羰基的典型反应是亲核加成反应。
加成(1)与氢氰酸的加成
醛、酮与氢氰酸发生加成反应生成α-羟基腈(又叫氰醇)。
羰基与氢氰酸的加成反应在有机合成上很有用,是增长碳链的方法之一。羟基腈是一类活泼化合物,易于转化成其他化合物,因而是有机合成中间体。例如,α-羟基腈可以水解成α-羟基酸,α-羟基酸进一步失水,变成α,β-不饱和酸。
丙酮与氢氰酸在氢氧化钠的水溶液中反应,生成丙酮氰醇,后者在硫酸存在下与甲醇作用,即发生水解、酯化、脱水反应,氰基变成甲氧酰基,最后生成甲基丙烯酸甲酯。甲基丙烯酸甲酯聚合生成聚甲基丙烯酸甲酯,即有机玻璃。
醛、酮与氢氰酸加成时,虽然可以直接用氢氰酸作反应试剂,但是它极易挥发,且毒性很大,所以操作要特别小心,需要在通风橱内进行。为了避免直接使用氢氰酸,常将醛、酮与氰化钾或氰化钠的水溶液混合,然后缓缓加入硫酸来制备氰醇,这样可以一边产生HCN,一边进行反应;也可以先将醛、酮与亚硫酸氢钠反应,再与氰化钠反应制备氰醇。
与格氏试剂(2)与格氏试剂的加成
在格氏试剂中,可以把R看作是负碳离子(R),它所起的作用与

、
、
等相似。由于负碳离子的亲核性很强,所以格氏试剂可以和大多数醛、酮发生加成反应,生成碳原子更多的、具有新碳架的醇。格氏试剂与甲醛作用生成伯醇,与其他醛作用生成仲醇,而格氏试剂与酮作用则生成叔醇。但当酮分子中的两个烃基和格氏试剂中的烃基体积都很大时,格氏试剂对羰基的加成可因空间位阻增加而大大减慢,相反却使副反应变得重要了,如空间位阻较大的二异丙基酮与叔丁基溴化镁加成时则有两种副反应产生,一种是二异丙基酮烯醇化得烯醇的镁化物。另一种副反应是羰基被还原成仲醇,格氏试剂中的烃基失去氢变成烯烃。在这种情况下,用活性更强的有机锂化合物代替格氏试剂,仍能得到加成产物,而且产率较高,并易分离。有机锂化合物和醛、酮反应的方式和与格氏试剂相似。例如和醛、酮反应,则分别得到仲醇或叔醇。与格氏试剂不同之处是,有机锂化合物和空间位阻较大的酮加成时,仍以加成产物为主。由于格氏试剂是活性很大的试剂,所以反应的第一步,即格氏试剂与羰基加成这一步,必须要在绝对无水的条件下进行反应。一般用经过干燥处理的乙醚作溶剂,极其微量的水存在都会导致反应的失败。
与醇的加成(3)与醇的加成
常温下羰基可与羟基发生可逆反应,生成半缩醛、半缩酮:

在有Lewis酸存在时,反应可进一步发生生成缩醛、缩酮:

此反应可用于羰基的保护
羰基化合物
结构和命名
羰基化合物的结构:
在醛(Aldehydes)和酮(Ketones)分子中,都含有一个共同的官能团——羰基,故统称为羰基化合物。醛分子中,羰基至少要与一个氢原子直接相连,故醛基一定位于链端。
羰基化合物的命名:
(1)普通命名法
醛按氧化后生成的羧酸命名,酮看作是甲酮的衍生物。
可用α、β、γ、δ等标记取代基位置。
(2)系统命名法
当分子中含有多种官能团时,首先要确定一个主官能团,然后,选含有主官能团及尽可能含较多官能团的最长碳链为主链。主链编号的原则是要让主官能团的位次尽可能小。命名时,根据主官能团确定母体的名称,其他官能团作为取代基用词头表示,分子中如涉及立体结构要在名称最前面表明其构型,然后根据名称的基本格式写出名称。
羰基化合物的物理性质
(1)沸点:羰基具有偶极矩,增加了分子间的吸引力,沸点比相应相对分子质量的烷烃高,但比醇低。
(2)水溶性:醛酮的氧原子可以与水形成氢键,因此低级醛酮能与水混溶。
羰基化合物的化学性质
亲核加成反应
(1)反应机理
反应过程中,一般是亲核试剂中带负电荷的部分(即亲核部分)先进攻底物中不饱和化学键带部分正电荷一端原子,并与之成键,π键断开形成另一端原子的负离子中间体,然后试剂中的亲电部分与负离子中间体结合,形成亲核加成产物。
最有代表性的反应是醛或酮的羰基与格氏试剂加成的反应:RC=O+R'MgCl→RR'C-OMgCl,再水解得醇,这是合成醇的良好办法。在羰基中,O稍显电负性;在格氏试剂中,C-Mg相连,Mg稍显电正性,C是亲核部位。于是格式试剂的亲核碳进攻亲电的羰基碳,双键打开,新的C-C键形成。
羰基可与碳为中心原子的亲核试剂加成,如格氏试剂、HCN、炔化钠。
羰基还可与氮为中心原子的亲核试剂的加成,如氨及其衍生物。
羰基还与氧为中心原子的亲核试剂的加成,如H2O、ROH等。
(2)反应应用——增长碳链
利用亲核加成反应增长碳链。
格氏试剂是含卤化镁的有机金属化合物,是一类亲核试剂,在有机合成中应用十分广泛。
格氏试剂可以合成氘代烃;格氏试剂与醛、酮、酯、环氧烷发生亲核加成反应成相应的醇;反应若生成二级醇,还可以氧化成酮,再继续与格氏试剂反应生成三级醇。格氏试剂与二氧化碳作用可制备多一个碳的羧酸。
α-活泼氢引起的反应
与官能团直接相连的碳叫α-碳,而α-碳上的氢即α-氢。α-氢的活性受与之直接相连的官能团或取代基的影响,通常会表现出特殊的反应活性,及比其他的氢的活性大,比较容易发生化学反应的特性和反应。
含有α-H的醛的存在下,在稀碱的存在下,可以互相结合生成β-羟醛基,受热后进而生成α、β-不饱和醛(有第二个α-H),通过羟醛缩合,在分子中形成了新的碳碳键,增长了碳链。
酮式、烯醇式的互变异构、醛酮的α-H卤代、卤仿反应、羟醛缩合反应等。
氧化和还原反应
(1)氧化反应
醛极易氧化,许多氧化剂都能将醛氧化成酸。脂肪醛比芳醛容易氧化。然而,将醛暴露在空气中,则是芳醛比脂肪醛容易氧化,这是因为用化学氧化剂氧化为离子型氧化反应。
酮遇一般氧化剂,抗拒氧化。酮遇强烈氧化剂,碳链断裂,形成酸。酮氧化时碳碳键断裂,一般生成混合物,意义不大,但是环酮氧化后可得单一化合物,在制备上有意义。
酮能发生一个特殊的氧化反应:拜耳-魏立格(Baeyer-Villiger)氧化,即酮类化合物被过酸氧化,与羰基直接相连的碳链断裂,插入一个氧形成酯的反应。
(2)还原反应
醛和酮在一定条件下经催化氧化可还原成醇,但需要注意:有些反应需要在加温、加压或有特殊催化剂才能进行;最常用的溶剂是醇;如羰基两侧的立体环境不同,催化剂通常从空阻小的一侧被吸附,顺型加氢。
其他反应
(1)Perkin反应
芳醛与含α-H的脂肪族酸酐,在相应的羧酸盐存在下共热,发生缩合生成α,β-不饱和酸,该反应称为珀金(Perkin)反应。
(2)Mannich反应
含有α-H的醛(酮),与甲醛和氨(或1°胺、2°胺)的盐酸盐之间发生的缩合反应,称为曼尼希(Mannich)反应。
该反应的净结果是二甲氨甲基取代了α-H,故又称为氨甲基化反应,产物为β-氨基酮。
Mannich反应通常是在酸性溶液中进行,除醛、酮外,其他含α-H的化合物如酯、腈等也可发生该反应。[1]

酮基