不可逆绝热过程是指热力学系统在状态变化时经历的一种理想过程。
不可逆绝热过程相关的文章
朝圣者是指参加朝圣的人们。朝圣者都是朝着他们认为的天堂方向朝拜的,一般都是庙宇和高山等。朝圣者目的地一般为耶路撒冷、麦加或西藏(分属世界三大宗教基督教、伊斯兰教、佛教)。朝圣者有不同的信仰,他们的朝圣之路都是通往他们内心认为的最神圣的地方。朝圣者在朝圣途中有五步一拜、十步一跪的礼仪。有不少朝圣者,在
黑海(英文名:Black Sea;俄文名:Чёрное море)是亚欧大陆西南部内陆海,北部与乌克兰接壤,东北部与俄罗斯接壤,东部与格鲁吉亚接壤,南部与土耳其接壤,西部与保加利亚和罗马尼亚接壤,经纬度范围为北纬46°33'至40°56,东经27°27'至41°42',面积约42.2万平方千米,平均
甜瓜(学名:Cucumis melo L.)是葫芦科(Cucurbitaceae)黄瓜属(Cucumis)植物,别名白兰瓜、哈密瓜、香瓜。甜瓜原产于印度和非洲国家,后广泛引种于世界温带至热带地区,中国各地广泛栽培。甜瓜喜光照,喜温耐热,常生长在土层深厚、通透性好、不易积水的沙土中。
尼罗河本词条是多义词,共5个义项流经非洲东部与北部的河流尼罗河,全长6670公里,是世界第一长河,非洲主河流之父。发源于东非高原,自南向北注入地中海,是一条国际河流。流经布隆迪、卢旺达、坦桑尼亚、乌干达、埃塞俄比亚、苏丹、埃及等7个国家,跨越世界上面积最大的撒哈拉沙漠。流域面积约335万平方公里,占非洲大陆面积的九分之一,年平均流量每秒3100立方米。尼罗河——阿拉伯语意为“大河”。“尼罗,尼罗,
提比略·恺撒·奥古斯都罗马帝国第二位皇帝提比略,全名提比略·恺撒·(神君奥古斯都之子·)奥古斯都(拉丁语:Tiberius Caesar Divi Augusti filius Augustus,公元前42年11月16日—公元37年3月16日),原名提比略·克劳狄乌斯·尼禄或提比略·尤里乌斯·恺撒(Tiberius Claudius Nero或Tiberius Julius Caesar),中文又
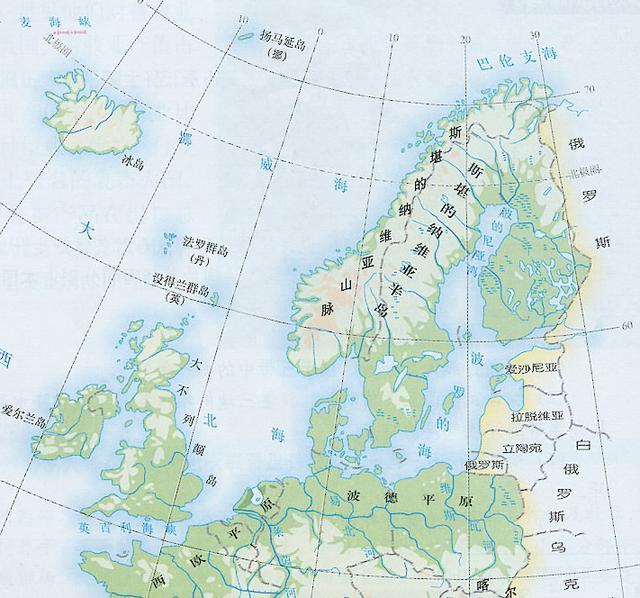
斯堪的纳维亚半岛(丹麦语:Skandinaviske halvø,瑞典语:Skandinaviska halvön,挪威语:Den skandinaviske halvøy,芬兰语:Skandinavian niemimaa),位于欧洲西北角,其濒临波罗的海、挪威海及北欧巴伦支海,与俄罗斯和芬兰北部接壤,北至芬兰,意为“斯堪的纳维亚人居住之地”。“斯堪的纳维亚”(Scandinavian)一词源自条顿语“skadino”,意为“黑暗”,再加上表示领土的后缀-via,全名意为“黑暗的地方”。因半岛 地处高纬

尚可名片
这家伙太懒了,什么都没写!