主要特性
普遍性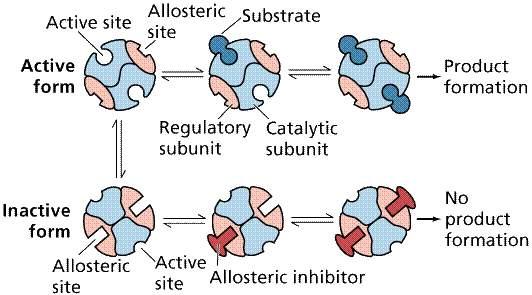
酶促反应
1、酶与一般催化剂一样,只催化热力学允许的化学反应(即可逆反应);2、可以加快化学反应的速度,而不改变反应的平衡点,即不改变反应的平衡常数;
3、作用机理都是降低反应的活化能;
4、在反应前后,酶没有质和量的改变,且微量的酶便可发挥巨大的催化作用。
特殊性但是酶也具有不同于其他催化剂的特殊性。
在酶促反应中,酶作为高效催化剂,使得反应以极快的速度或在一般情况无法反应的条件下进行。
酶是生物体内进行各种化学反应最重要的物质。
特点一、酶促反应具有极高的效率
二、酶促反应具有高度的特异性
酶的特异性是指酶对底物的选择性,有以下三种类型:
1.绝对特异性酶只作用于特定结构的底物,生成一种特定结构的产物。如淀粉酶只作用淀粉。
2.相对特异性酶可作用于一类化合物或一种化学键。例如磷酸酶可作用于所有含磷酸酯键的化合物。
3.立体异构特异性一种产仅作用于立体异构体中的一种。例如L-乳酸脱氢酶只作用于L-乳酸,而对D-乳酸不起催物作用。
三、酶活性的可调节性
四、酶活性的不稳定性
因素
温度、酸碱度、酶的浓度、被催化物质的浓度、抑制剂、激活剂、反应产物底物浓度对酶反应速度的影响底物浓度的改变,对酶反应速度的影响比较复杂。在一定的酶浓度下当底物浓度较低时
(底物浓度从0逐渐增高),反应速度与底物浓度的关系呈正比关系(如右图);随着底物浓度的增加,反应速度不再按正比升高;如果再继续加大底物浓度,反应速度却不再上升,趋向一个极限。
影响
在一定的温度和pH条件下,当底物浓度足以使酶饱和的情况下,酶的浓度与酶促反应速度呈正比关系。
pH对酶反应速度的影响
pH对酶促反应速度的影响酶反应介质的pH可影响酶分子,特别是活性中心上必需基团的解离程度和催化基团中质子供体或质子受体所需的离子化状态,也可影响底物和辅酶的解离程度,从而影响酶与底物的结合。只有在特定的pH条件下,酶、底物和辅酶的解离情况,最适宜于它们互相结合,并发生催化作用,使酶促反应速度达最大值,这种pH值称为酶的最适pH。
胰蛋白酶大部分酶的活力受其环境pH的影响,在一定pH下,酶促反应具有最大速度,高于或低于此值,反应就会下降,通常称此pH为酶的最适pH。不同酶的最适pH不同。
右图:例如:胃蛋白酶的最适pH为1.5~2.2,胰蛋白酶的最适pH为8.0~9.0,唾液淀粉酶的最适pH为6.8等。动物酶多在pH6.5~8.0之间,植物及微生物多在pH4.5~6.5之间,但也有例外。如:真菌的最适pH为5.0~6.0,多数细菌的最适为6.5~7.5,放线菌的最适在7.5~8.5。
体内多数酶的最适pH值接近中性,但也有例外,如胃蛋白酶的最适pH约1.8,肝精氨酸酶最适pH约为9.8。溶液的pH值高于和低于最适pH时都会使酶的活性降低,远离最适pH值时甚至导致酶的变性失活(图)。所以测定酶的活性时,应选用适宜的缓冲液,以保持酶活性的相对恒定。临床上根据胃蛋白酶的最适PH偏酸这一特点,配制助消化的胃蛋白酶合剂时加入一定量的稀盐酸,使其发挥更好的疗效。
pH影响酶活性的主要原因
过酸、过碱影响了酶分子的结构,甚至使酶变性失活。
应该注意的是,酶在试管中的最适pH与它在正常细胞中的生理pH值并不一定完全相同。这是因为一个细胞内可能会有几百种酶,不同的酶对此细胞内的生理pH的敏感性不同;也就是说此pH对一些酶是最适pH,而对另一些酶则不是,不同的酶表现出不同的活性。这种不同对于控制细胞内复杂的代谢途径可能具有很重要的意义。
温度对酶促反应速度的影响
化学反应的速度随温度增高而加快,但酶是蛋白质,可随温度的升高而变性。在温度较低时,前一影响较大,反应速度随温度升高而加快。但温度超过一定范围后,酶受热变性的因素占优势,反应速度反而随温度上升而减慢。常将酶促反应速度最大的某一温度范围,称为酶的最适温度。
人体内酶的最适温度接近体温,一般为37℃~40℃之间,若将酶加热到60℃即开始变性,超过80℃,酶的变性不可逆。
温度对酶促反应速度的影响在临床实践中具有指导意义。低温条件下,酶的活性下降,但低温一般不破坏酶,温度回升后,酶又恢复活性。所以在管理技术操作中对酶制剂和酶检测标本(如血清等)应放在冰箱中低温保存,需要时从冰箱取出,在室温条件下等温度回升后再使用或检测。温度超过80℃后,多数酶变性失活,临床应用这一原理进行高温灭菌。
酶的最适温度与反应所需时间有关,酶可以在短时间内耐受较高的温度,相反,延长反应时间,最适温度便降低。据此,在生化检验中,可以采取适当提高温度,缩短时间的方法,进行酶的快速检测。
不同的温度对活性的影响不同,但都有一个最适温度。在最适温度的两侧,反应速度都比较低。
温度对酶促反应的影响包括两方面:一方面是当温度升高时,反应速度也加快,这与一般化学反应相同。另一方面,随温度升高而使酶逐步变性,即通过减少有活性的酶而降低酶的反应速度。在低于最适温度时,前一种效应为主,在高于最适温度时,则后一种效应为主,因而酶活性丧失,反应速度下降。
在制备培养基的过程中,可采用高温对培养基进行灭菌,主要是破坏了微生物体内的酶的活性。采用高温灭菌在医学和生活实践中都有较广泛的应用。
在低温的条件下,酶的活性降低,但酶分子的结构一般还会发生改变。所以,人们可以选择在低温下保存酶。在生活实践中人们也经常选择在低温下较长时间保存食品。
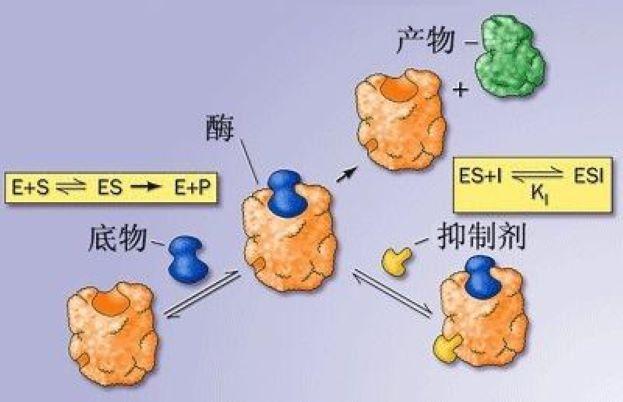
抑制剂的作用
通过改变酶必需基团的化学性质从而引起酶活力降低或丧失的作用称为抑制作用,具有抑制作用的物质称为抑制剂,抑制剂通常是小分子化合物,但在生物体内也存在生物大分子类型的抑制剂。
酶的抑制剂分类
酶的抑制剂分为不可逆抑制剂和可逆抑制剂两大类。不可逆抑制剂与酶的必需基团以共价键结合,引起酶的永久性失活,其抑制作用不能够用透析,超滤等温和物理手段解除。可逆抑制剂与酶蛋白以非共价键结合,引起酶活性暂时性丧失,其抑制作用可以通过透析、超滤等手段解除。可逆抑制剂又分为竞争性抑制剂、非竞争性抑制剂和反竞争性抑制剂等。
激活剂的作用
酶的活力可以被某些物质提高,这些物质称为激活剂,在酶促反应体现中加入激活剂可导致反应速率增加。通常酶对激活剂有一定选择性,且有一定浓度要求,一种酶的激活剂对另一种酶可能是抑制剂,当激活剂的浓度超过一定的范围时,它就成为抑制剂。