定义
多环芳烃
多环芳烃定义:含有一个苯环以上的芳香化合物,产生于工业生产、有机物热解或不完全燃烧,其中有许多被证明具有致癌毒性。应用学科:生态学(一级学科);污染生态学(二级学科)
同类物质
PAHs主要包括18种同类物质:
18种常见多环芳烃
⒈NAP Naphthalene 萘(NAP)
2 .ANY Acenaphthylene 苊烯(ANY)
3.Acenaphthene 苊萘嵌戊烷(ANA)
⒋FLU Fluorene 芴(FLU)
⒌PHE Phenanthrene 菲(PHE)
⒍ANT Anthracene 蒽(ANT)
⒎FLT Fluoranthene 荧蒽(FLT)
⒏PYR Pyrene 芘(PYR)
⒐BaA Benzo(a)anthracene 苯并(a)蒽(BaA)
⒑CHR Chrysene 䓛(CHR)
⒒ BbF Benzo(b)fluoranthene 苯并(b)荧蒽(BbF)
⒓ BKF Benzo(k)fluoranthene 苯并 (k)荧蒽(BkF)
⒔BaP Benzo(a)pyrene 苯并(a)芘(BaP)
⒕IPY Indeno(1,2,3-cd)pyrene 茚苯(1,2,3-cd)芘(IPY)
⒖DBA Dibenzo(a,h)anthracene 二苯并(a,h)蒽(DBA)
⒗BPE Benzo(g,hi)perylene 苯并(ghi)北(二萘嵌苯)(BPE)
17.Benzp(e)pyrene 苯并(e)芘(BeP)
18.Benzo(j)fluoranthene 苯并(j)荧蒽(BjF)
物质来源
在自然界中这类化合物存在着生物降解、水解、光作用裂解等消除方式,使得环境中的PAHs含量始终有一个动态的平衡,从而保持在一个较低的浓度水平上,但是近些年来,随着人类生产活动的加剧,破坏了其在环境中的动态平衡,使环境中的PAHs大量的增加。
自然源在人类出现之前,自然界也存在天然源,主要来自陆地、水生植物和微生物的生物合成过程,另外森林、草原的天然火灾及火山的喷发物和从化石燃料、木质素和底泥中也存在多环芳烃,这些构成了PAH的天然本底值。通常土壤的PAH本底值为100~1000μg/kg。淡水湖泊中PAH的本底值为0.01~0.025μg/L,地下水中PAH的本底值为0.001~0.01μg/L,大气中PAH的本底值为0.1~0.5ng/m。
人为源PAHs人为源来自于工业工艺过程、缺氧燃烧、垃圾焚烧和填埋、食品制作及直接的交通排放和同时伴随的轮胎磨损、路面磨损产生的沥青颗粒以及道路扬尘中,其数量随着工业生产的发展大大增加,占环境中多环芳烃总量的绝大部分;溢油事件也成为PAHs人为源的一部分。因此,如何加快PAHs在环境中的消除速度,减少PAHs对环境的污染等问题,日益引起人们的注意。
分类
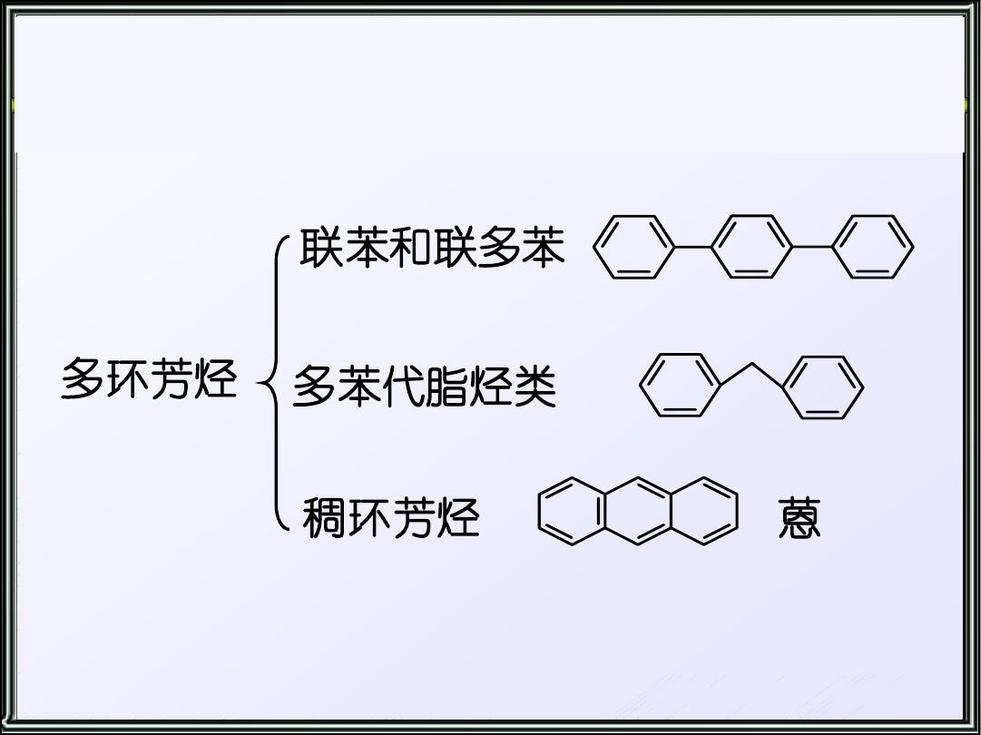
根据苯环的连接方式不同,多环芳烃分为联苯和联多苯类、多苯代脂肪烃类和稠环芳烃类。
联苯和联多苯类苯环间以σ键连接成的化合物称为联苯。联苯类衍生物及联多苯类化合物都是以联苯为母体命名。结构和性质与单环芳烃相似。
多苯代脂肪烃多苯代脂肪烃类由若干个苯环取代脂肪烃中的氢原子而形成的化合物。此类化合物以苯基作为取代基,脂肪烃为母体来命名。结构和性质与单环芳烃相似。

多环芳烃
稠环芳烃稠环芳烃是指两个或两个以上的苯环共用两个相邻碳原子稠合而成。
萘是煤焦油中含量最多的化合物,在高温煤焦油中约含10%,萘的分子式是C10H8,它是两个苯环共用相邻两个碳原子稠合而成。萘是白色片状晶体,熔点80℃,沸点218℃,不溶于水,易溶于热的酒精、乙醚等有机溶剂。易挥发、易升华、有特殊气味。
蒽存在于煤焦油中,含量约为0.25%。蒽的分子式为C14H10,由三个苯环稠合而成。菲也存在于煤焦油中,与蒽互为同分异构体。

稠环芳烃
其他稠环芳烃芳烃主要来自于煤焦油中,其中可分离出稠环芳烃,如茚、芴、苊是脂环和芳环相稠合的芳烃,四苯、芘等是高级稠环芳烃。此外,蒽和菲的衍生物是具有显著致癌作用的稠环芳烃,简称致癌烃。
物质变化
存在状态多环芳烃广泛存在于人类生活的自然环境如大气、水体、土壤、作物和食品中。截止2013年4月份己知的多环芳烃约有200多种。大气中的PAHs以气、固两种形式存在,其中分子量小的2-3环PAHs主要以气态形式存在,4环PAHs在气态、颗粒态中的分配基本相同,5-7环的大分子量PAHs则绝大部分以颗粒态形式存在。水体中的多环芳烃可呈三种状态:吸附在悬浮性固体上;溶解于水;呈乳化状态。己知的地表水中的多环芳烃有20余种。地下水和海水中也检测了多环芳烃。土壤中PAHs的浓度一般在10-10µg/Kg范围内,城郊土壤中PAHs的浓度更高,达10-10µg/Kg。土壤的污染必然影响到作物的生长。蔬菜中BPa的含量以叶类蔬菜最多,根菜类和果实类蔬菜次之
迁移变化多环芳烃在环境中大多数是以吸附态和乳化态形式存在,一旦进入环境,便受到各种自然界固有过程的影响,发生变迁。通过复杂的物理迁移、化学及生物转化反应,在大气、水体、土壤、生物体等系统中不断变化,改变分布状况。处在不同状态、不同系统中的多环芳烃则表现出不同的变化行为。多环芳烃进入大气后,可通过化学反应、降尘、降雨、降雪等过程进入土壤及水体中。
特性
物理性质多环芳烃大部分是无色或淡黄色的结晶,个别具深色,熔点及沸点较高,蒸气压很小,大多不溶于水,易溶于苯类芳香性溶剂中,微溶于其他有机溶剂中,辛醇-水分配系数比较高。多环芳烃大多具有大的共扼体系,因此其溶液具有一定荧光。一般说来,随多环芳烃分子量的增加,熔沸点升高,蒸气压减小。多环芳烃的颜色、荧光性和溶解性主要与多环芳烃的共扼体系和分子苯环的排列方式有关。随p电子数的增多和p电子离域性的增强,颜色加深、荧光性增强,紫外吸收光谱中的最大吸收波长也明显向长波方向移动;对直线状的多环芳烃,苯环数增多,辛醇-水分配系数增加,对苯环数相同的多环芳烃,苯环结构越“团簇”辛醇-水分配系数越大。
化学性质多环芳烃化学性质稳定。当它们发生反应时,趋向保留它们的共扼环状系,一般多通过亲电取代反应形成衍生物并代谢为最终致癌物的活泼形式。其基本单元是苯环,但化学性质与苯并不完全相似。分为以下几类:
⑴具有稠合多苯结构的化合物

x电子分布与苯类似的多环芳烃
如三亚苯、二苯并 [e,i]芘、四苯并 [a,c,h,j]蒽等,与苯有相似的化学稳定性,说明:电子在这些多环芳烃中的分布是和苯类似的。如图1所示:图1x电子分布与苯类似的多环芳烃
⑵呈直线排列的多环芳烃
如蒽、丁省、戊省等,比苯的化学性质活泼得多。其反应活性随环的增加而变强,环数达到7个的庚省,化学性质极为活泼,几乎无法获得纯品。这种多环芳烃进行化学反应的特点,是常在相当于蒽的中间一个苯环的相对碳位(简称中蒽位)上发生。如图2所示:
⑶呈角状排列的多环芳烃
如菲、苯并[a]慈、蔡并[2,3-a]蒽、蕙并,[2,3-a]蕙等,其化学活性一般比相应的直线排列的异构体小。在加合反应中,通常在相当于菲的中间的双键部位,即菲的9,10键(简称中菲键)上进行。π电子在很大程度上被限定在中菲键上,因此中菲键的化学性质非常接近于烯键。角状多环芳烃含有4个以上环的,除了较活泼的中菲键外,还常含有直线多环芳烃类似的活泼对位——中慈位,如苯并[a]葱的8,15位。但活泼程度比相应的直线状异构体低,基本上也是随环数的增多而增强 如图3所示:
⑷结构更复杂的稠环烃
如苯并[a]花、二苯并[a,i]芘等,具有活泼的中菲键,但没有活泼的对位。这类多环芳烃中具有致癌性的不少,如苯并[a]芘是致癌性最强的多环芳烃。它们的结构如图4所示:

复杂多环芳烃
分析方法
随着科学技术的不断进步,多环芳烃的检测方法也在不断地发展变化,从开始的柱吸附色谱、纸色谱、薄层色谱(TLC)和凝胶渗透色谱(GPC)发展到如今的气相色谱(GC)、反相高效液相色谱(RP-HPLC),还有紫外吸收光谱(UV)和发射光谱(包括荧光、磷光和低温发光等),还有质谱分析、核磁共振和红外光谱技术,以及各种分析方法之间的联用技术等。较为常用的是分光光度法和反相高效液相色谱法。近几年来多环芳烃的分析方法发展迅速,出现了如微波辅助溶剂萃取、固相微萃取、超临界流体等多种新的分析技术。
分光光度法分光光度法有紫外分光光度法、荧光光谱法、磷光法,低温发光光谱法和一些新的发光分析法等等。用发光技术分析RAHs多环芳烃样品比吸收分光光度法具有灵敏度高、专属性强等优点。发光法的灵敏度比吸收法高10-100倍,其检出量约在10.6一10.8g范围。由于紫外分光光度法仪器简单,通用性强,所以也比较常见。一般PAHs的mole吸光系数(ε)在10-10左右,检出灵敏度约在µg数量级。下表1是部分多环芳烃的最大紫外吸收波长。
表1 部分多环芳烃的最大紫外吸收波
物质 最大吸收波长(nm)
──────────────────────────────────
萘 275
蒽 370
丁省 460
戊省 580
低温荧光分析法是近几年出现的一种新的多环芳烃分析方法。于立军等利用光纤传导低温装置和荧光分光光度计偶联,对多环芳烃进行低温激发、发射光谱扫描,获得了多环芳烃的Shpolskii低温荧光光谱,呈现出很明显的精细结构,对多环芳烃有很好的鉴别能力。
物理方法⑴加热法
水中的苯并[a]芘可通过加热煮沸使其浓度降低,当加热至沸时,其含量可减少37%-57%,如再继续加热,则其含量不再减少,且发现部分苯并[a]芘已转入到加热煮沸形成的沉垢中去。其他多环芳烃也可在加热煮沸过程中部分地被除去。
⑵混凝沉淀法
利用此法及氯化可除去15%一85%的苯并[a]芘,如果再用合成絮凝剂及通过活性炭过滤,所得到的处理水,其多环芳烃的含量可达到食用水的标准。
⑶吸附法
石化厂排出的废水中的荧蒽、苯并[al芘、茚并芘、3,4-苯并荧蒽、11,12-苯并荧蒽、苝及苝等,可以用活性炭吸附去除。使用粉状活性炭,虽然可以降低其臭味,但是要达到饮用水的标准,即0.2µg/L是相当困难的。活性炭对分子量大的多环芳烃吸附效果较差,采用大孔树脂吸附效果较好。总的来说,仅用物理方法处理多环芳烃是困难的,应当结合生化处理方法和化学处理方法一起使用。
化学方法化学法处理多环芳烃主要有光氧化及化学药剂氧化两大类。
在光氧化过程中,水中的多环芳烃是在光诱发所产生的单线态氧、臭氧或轻基游离基的作用下发生氧化降解的。苯并[a]芘可因光氧化而去除56%,并形成苯并[a]芘-3,6-二酮或其他二酮类化合物,以及一些未知的化合物。
在化学氧化中,主要是臭氧氧化和氯氧化两种。臭氧去除多环芳烃的效果比其它氧化法为好。水溶液中的4µg/L的苯并[a]芘用2.5µg/L臭氧处理3分钟,则其残余量为0.06µg/L;用0.45mg/L的臭氧处理5分钟,则残余量为0.04µg/L。增加臭氧浓度,延长作用时间,可以提高去除率,但残余量总不会低于0.02µg/L 乌锡康。
薄层色谱
薄层色谱法又称薄层层析法,包括吸附薄层和分配薄层。其优点是展开时间短、可使用腐蚀性显色剂、斑点密度很大而易于检测、展开后斑点中的样品可被提取以便采用分光光度法来测定、可作为制备色谱的预实验方法等。
⑴吸附薄层
各种吸附剂的表面都存在着吸附活性,对有机化合物表现出程度不同的吸附能力,正是利用混合物中不同组分的分子、溶剂分子与吸附剂表面分子间的相互作用不同,用一定的溶剂系统(流动相)展开,由于溶剂与混合物里的各组分争夺吸附剂活性表面,发生了吸附与解吸附的可逆过程,随着流动相的移动,这一过程不断进行,使得各组分在两相间的迁移速度不同而移动不同的距离,从而达到分离的目的。
不同的化合物由于结构性质上的差异,展开剂对它们的洗脱能力和在吸附剂上的吸附、解吸附性能也是不同的。因而在吸附剂上移动的距离也就不会相同,形成各种组分彼此程度不同地分离,性质差异愈大,分离效果愈好。
⑵分配薄层
分配薄层是利用物质在互不相溶的两相溶剂中分配系数不同而达到分离的一种方法。它的基本原理来自两相逆流萃取,是以一种多孔物质作为支持剂(这一点不同于吸附薄层的吸附剂),将极性溶剂在层析过程中始终固定在支持剂上,称为固定相,另用一与固定相不相混溶的溶剂洗脱,称为移动相。被分离的物质在固定相和移动相之间不断地作连续的动态的分配,利用不同成分在两相间分配系数不同而达到分离的目的。
反相高效液相色谱法(RP.HPPLC)
高效液相色谱法(HPLC)可在常温下工作、对PAHs分辨率和灵敏度高、柱后馏分便于收集、适合荧光检测器分析等优点,已广泛应用于PAHs的分离和定量中,特别对多环、高相对分子质量的PAHs具有优势。美国EPA推荐使用乙腈和水作为HPLC 的流动相,但乙腈价格较贵,且有毒性,贾瑞宝采用甲醇和水作为流动相进行梯度淋洗,16种PAHs的加标回收率为79%-104%,相对标准偏差5.2%-19.5%,适于PAHs的检测。林琳等采用微波提取高效液相色谱法测定土壤中的多环芳烃,检出限为0.10-0.80µg/kg,相对标准偏差为0.60%-4.60%,回收率为58.1%-97.8%。陶敬奇等采用固相微萃取高效液相色谱联用测定水样中8种多环芳烃,通过对萃取和解吸条件的优化,方法的检出限为0.002- 0.180µg/L,相对标准偏差为4.4%-2.2%,回收率为91.1%- 115.8%,是一种快速分析环境水样中痕量多环芳烃的方法。
其他研究
研究方向环境中难降解有机物的生物去除,特别是多环芳烃的生物降解是环境科学家们共同关心的问题。尽管微生物修复是清除多环芳烃污染的最有效的手段,但是该技术要成功应用于实际,还是受到多种因素的限制。多环芳烃结构的特殊性及其低水溶性限制了它们被土著微生物的降解。以下几个方面是值得深入研究的方向:
⑴ 分离能以四环以上高分子量多环芳烃作为唯一碳源的高效降解菌株,研究生物降解的影响因素,提高现有菌种的生物降解能力。
⑵ 多环芳烃的微生物降解途径和机理与降解过程中的共代谢机理研究,降解过程的中间步骤和降解过程中积累的中间产物的结构性质,深入研究某些降解产物的毒性。
⑶ 通过遗传工程技术,把编码降解污染物酶的质粒或是基因,整合到能在污染环境生长存活的土著微生物的DNA 中,使其获得较强的污染物降解能力,充分发挥生物修复的作用。
⑷微生物与植物联合修复的根际机理研究,多环芳烃污染土壤的植物修复正处于起步阶段,而微生物与植物联合修复将是一种很有发展前途的新型修复技术。
⑸ 深入研究生物表面活性剂产生的机理及其在实际处理中的应用,环境因子对多环芳烃生物降解的影响等一系列与实际污染土壤和地下水生物修复工程相关的问题。
致癌毒性多环芳烃英文简称PAHs,是强致癌物质,可通过接触导致人体致癌。在已知的500多种致癌物中,有200多种和多环芳烃有关,已成为癌症的代名词。
多环芳烃(PAHs)是指具有两个或两个以上苯环的一类有机化合物。多环芳烃是分子中含有两个以上苯环的碳氢化合物,包括萘、蒽、菲、芘等150余种化合物。英文全称为polycyclic aromatic hydrocarbon,简称PAHs。国际癌研究中心(IARC)(1976年)列出的94种对实验动物致癌的化合物。其中15种属于多环芳烃,由于苯并a芘是第一个被发现的环境化学致癌物,而且致癌性很强,故常以苯并(a)芘作为多环芳的代表,它占全部致癌性多环芳烃1%-20%。
政策
截至2011年11月,各国家地区通过书面法律或法令确定下来的有:
欧盟76/769/EEC;
德国German:GS认证、LFGB;
美国US:EPA;
中国:GB,GB/T,GHZ
毒性与危害
随着其环数增加、化学结构的变化和疏水性的增强,其电化学稳定性、持久性、抗生物降解能力和致癌性会增大,挥发性也会随着其分子量的增加而降低。多环芳烃在自然界许多生物链都存在生物积累效应,其在自然界中的含量相当惊人,因此也被认定为影响人类健康的主要有机污染物。 PAHs对人体的呼吸系统、循环系统、神经系统损伤,对肝脏、肾脏等也会造成损害。
呼吸系统损伤工作场所中的 PAHs及其他有害物质多附着于可吸入性颗粒物上,随着呼吸运动进入呼吸道而入侵机体。大多数职业接触 PAHs 工人进行职业健康检查时均有不同程度的咽部红肿、咯痰增多的现象。有研究发现,苯并[a]芘可以降低肺泡表面活性物质的活力并且对其稳定性有一定程度的影响;同时 PAHs 对离体培养的支气管上皮细胞的线粒体抗凋亡能力有削弱作用。且在早期接触芘的情况下,非过敏体质的儿童呼吸道易感性增加。研究发现,PAHs代谢产物中的羟基菲和 1-羟基芘 (1-Hydroxypyrene,1-OHP)的蓄积作用与焦炉工第 1秒用力呼气量占肺活量比值呈负相关,且随年龄增长,肺功能下降越明显。表明职业性接触 PAHs 可导致工人肺功能下降,推测其中的菲和芘可能是引起职业性接触 PAHs 工人肺部早期损伤的主要物质。
循环系统损伤心率变异性 (Heartrate variability,HRV)降低是心脏自主神经功能紊乱的标志,可独立作为预测心血管疾病死亡率的指标。有研究显示,焦化厂接触 PAHs 工人的红细胞计数、中性粒细胞、红细胞比容水平和淋巴细胞 Olive尾距与尿中1-OHP、苯巯基尿酸水平相关,提示 PAHs 和苯混合接触可引起焦炉作业工人的周围血血象发生一定程度改变及淋巴细胞DNA损伤。
神经系统损伤PAHs受到关注以来,既往研究多集中探讨PAHs对儿童神经发育的影响,而对职业人群神经系统毒性的报道不多见。职业接触方面, PAHs 和铅联合接触可以影响16个基因及蛋白,其中包括14 个与神经系统疾病有关的蛋白和基因,这些基因和蛋白通过配体激活、细胞凋亡、氧化应激及炎性介质等途径对神经系统造成损伤。
肝脏损害肝脏血流丰富,是人体的主要代谢器官,对毒物具有一定的解毒功能。有研究以1-OHP作为职业接触 PAHs 的生物标志物,对焦炉工人进行肝脏功能损伤评估,发现肝脏生化指标与血红素结合蛋白有相关关系,血红素结合蛋白水平在低、中、高水平 PAHs 接触组间比较,差异均有统计学意义( P < 0. 05),且表达与接触程度存在弱相关,提示焦炉工人有肝脏损伤的可能。李济超等研究显示,职业接触PAHs 与脂肪肝密切相关,且随着环境中有害物质水平的升高,比值比也增高,提示职业接触PAHs可增加工人发生脂肪肝的危险性。
肾脏损害血尿酸和尿β2 -微球蛋白(β2 -Microglobulin,β2 -MG)是反映肾脏功能的指标,对发现早期肾损害有重要意义。有研究发现焦炉工尿β2 -MG水平高于对照组( P < 0. 05) ,提示接触PAHs的工人存在一定程度的肾脏损害。
降解方法
将多环芳烃(PAHs)从环境中去除被认为是恢复污染环境最重要的方法。许多物理处理和化学处理方法已经尝试过,其中包括焚烧法、碱催化脱氯、紫外线氧化、固定、溶剂萃取等,但这类方法存在成本高、较复杂、难以进行调控等弊端。此外,这些传统环境修复技术在许多情况下难以将这些污染物完全去除,而只是把它们从一个环境中转移到另一种环境中或者形成另一种污染物。目前,生物修复和半导体光催化降解技术是除去多环芳烃较好的方法。
生物修复目前微生物修复已经成为修复环境和去除包括多环芳烃在内许多污染物的重要技术。与高分子量多环芳烃相比,低分子量的多环芳烃相对稳定性较差,更易溶于水,因此也更易被微生物降解。细菌经过三十亿年的进化已经具备代谢几乎所有化合物获取能量的能力,并已被视为自然的终极清除剂。由于细菌具有较强的适应性,已被广泛用于降低或修复污染环境的危害。目前已发现的多环芳烃降解菌有很多种,其中萘和菲降解菌的研究更为广泛。细菌通常在有氧条件下降解 PAHs,主要通过加氧酶进行代谢,加氧酶主要包括单加氧酶或双加氧酶。细菌降解 PAHs 的第一步是通过双加氧酶使苯环上的碳原子发生羟基化作用形成顺式二氢醇,在二醇脱氢酶的作用下形成二醇中间体,通过内源或外源双加氧裂解酶通过邻位裂解或次裂解途径将二醇中间体雌二醇进行裂解反应形成中间体(如儿茶酚),最终转化为TCA循环中间体。真菌能够通过共同代谢作用将 PAHs 代谢为多种氧化产物或者二氧化碳。真菌对 PAHs 的降解作用主要通过单加氧酶进行降解。然而,真菌对 PAHs 的降解作用只是限于特定的菌株和生长条件才有效。能够降解多环芳烃的真菌主要有两类:木质素降解菌(白腐真菌)和非木质素降解菌。
半导体光催化降解半导体光催化降解法具有操作简单、可在常温常压下进行、能彻底矿化有机物等优点,在 PAHs等持久性有机污染物的治理中具有良好的应用前景。TiO2是一种高活性的半导体光催化剂,在降解 PAHs的研究中得到了广泛应用。将分散相的TiO2颗粒悬浮在污染物水溶液中,通过紫外光照射进行光催化反应,由于催化剂颗粒物与反应物的接触面积大,因此具有很高的降解效率。氮原子改性的TiO2在可见光区有较高的响应,这是由于N原子的引入导致 TiO2的带隙变窄,可见光照射8h后,萘在N-TiO2催化下的降解效率约为 80%,降解效率大幅度提高。

半导体光催化降解原理











